| |
|
| |
|
| |
| |
| ■ 制品内容 |
| 1. Probe qPCR Mix, with UNG (2×conc.) |
625 μl |
×2 |
| 2. Lentivirus Primer/Probe Mix for Provirus (10×conc.) |
250 μl |
|
| 3. hIFNg Primer/Probe Mix for Provirus (10×conc.) |
250 μl |
|
| 4. H2O |
1 ml |
|
| 5. ROX Reference Dye (50×conc.) |
200 μl |
|
| 6. ROX Reference Dye II (50×conc.) |
200 μl |
|
| 7. Provirus Control Template (4.13×107 copies/μl) |
25 μl |
|
| 8. EASY Dilution (for Real Time PCR) |
1 ml |
×2 |
|
| |
| ■ 制品说明 |
LVpro Provirus qPCR Quantitation Kit是利用Real Time PCR技术,检测使用慢病毒载体向人细胞导入基因时整合到基因组中的载体拷贝数(前病毒拷贝数)的制品。本制品可测定使用市面上广泛使用的慢病毒载体进行基因导入的人正常细胞的前病毒拷贝数。
|
| |
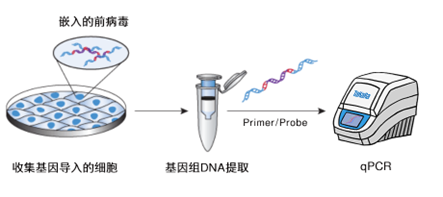 |
| 图1. LVpro Provirus qPCR Quantitation Kit的操作流程 |
Provirus Control Template包含1个拷贝的慢病毒序列和人IFNγ序列的一部分,分别制作两者的标准曲线,通过定量目的样品中基因组DNA中慢病毒和人IFNγ的拷贝数 (copies/μl),计算出每个细胞的平均前病毒拷贝数。
|
| |
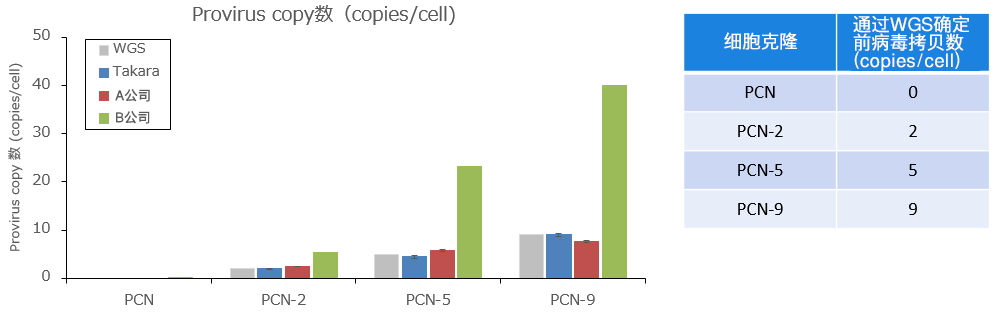 |
| Takara Bio Inc.比较结果
|
| 图2. 前病毒拷贝数的测定结果 (与WGS·其他公司比较) |
用慢病毒载体基因导入的细胞克隆 (常染色体2倍体细胞),从提取的基因组DNA中通过全基因组序列 (WGS) 确定前病毒拷贝数。另外,从各个细胞克隆中提取100 ng基因组DNA,通过本产品或其他公司的产品测定前病毒拷贝数。本产品和A公司产品显示的是3次独立试验的平均值。
结果显示,本产品检测的前病毒拷贝数和通过WGS得到的前病毒拷贝数几乎相同,表明本产品的定量非常正确。
|
| |
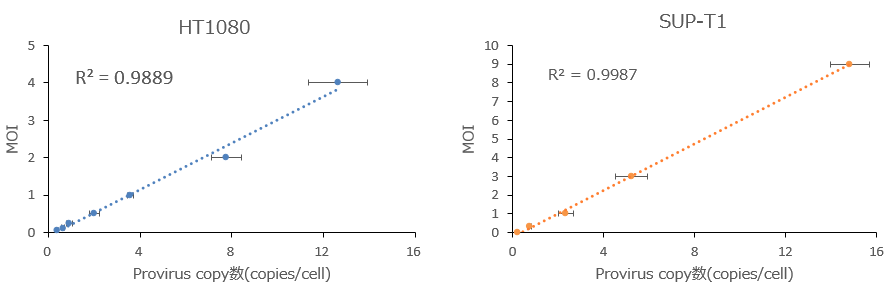 |
| 图3. MOI与前病毒拷贝数的相关性 |
(左) 将携带ZsGreen1基因的慢病毒载体逐级稀释,用不同MOI (Multiplicity of Infection) 感染HT1080细胞。
感染3天后,用DNase I处理细胞,然后用Nucleospin Tissue提取基因组DNA。
(右) 将携带CD19-CAR基因的慢病毒载体逐级稀释,用不同MOI感染SUP-T1细胞。
感染3天后,用DNase I处理细胞,然后用Nucleospin Tissue提取基因组DNA。
使用本产品,对每个样品使用100 ng基因组DNA进行实时PCR。确认了每个细胞的平均前病毒拷贝数与MOI之间的相关性。显示数据是3次独立检测的平均值。
结果显示,在不同细胞系和不同携带基因的不同组合中,MOI和前病毒拷贝数的R2值超过0.98,呈现高度相关性。 |
| |
| ■ 保存 |
-20℃
|
| |
| |

