| 新品 | 支原体检测简易指南 |
| 定期筛查是避免支原体污染的最有效方法 |
| 支原体(Mycoplasma)是一类特别的原核微生物,其缺乏细胞壁、形态多变并且能够轻松穿过标准的0.2微米滤膜,可通过直接接触或气溶胶远距离等方式进行传播,成为医学、生物研究和工业生产中不可忽视的污染源。 |
| ★ 医学领域 |
| 引发呼吸道、泌尿生殖道感染,易被误诊为病毒性疾病。 慢性感染可能导致免疫系统紊乱(如类风湿关节炎)。 |
| ★ 生物实验与生产 |
| 细胞培养污染:导致细胞代谢异常、基因表达改变、实验数据失真。 生物制品污染:疫苗、单克隆抗体生产中可能引入支原体,威胁产品安全性。 |
| ★ 常见致病种包括 |
| 肺炎支原体(M. pneumoniae):引发非典型肺炎。 生殖支原体(M. genitalium):与尿道炎、盆腔炎相关。 猪鼻支原体(M. hyorhinis):实验室细胞培养常见污染物。 |
| 作为兼性厌氧菌,支原体能在各种温度、氧气水平和其他恶劣条件下存活,包括暴露于液氮中。但支原体感染的鉴定异常困难,因受感染的培养物不会产生任何明显的视觉指标(如培养基的颜色或浑浊度变化),使得支原体能够在细胞培养物中长期存活而不被发现。因此,避免污染最有效的方法就是定期筛查,以尽快识别和分离潜在的支原体。 |
| 常见的支原体筛查检测方法 |
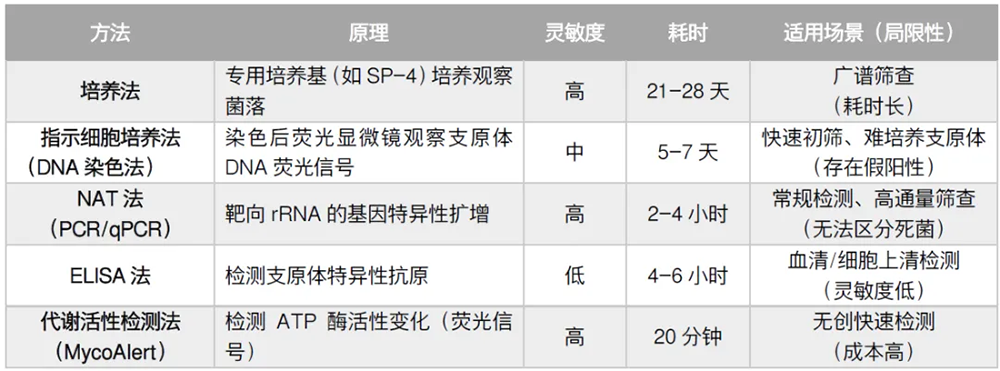 |
| 培养法和指示细胞法因其检测周期长或灵敏度问题,致使企业生产或产品放行周期拉长。细胞和基因疗法以及生物制剂的放行都要求进行支原体检测,随着细胞基因治疗的发展,行业内对支原体检测时效性和灵敏度要求也越来越高。基于PCR原理的支原体检测接受度不断提高,支原体检测正逐步将核酸扩增技术(NAT)作为黄金标准。 在中国药典(2020版)支原体检测中规定使用培养法和指示细胞培养法对支原体进行检测。虽未明确列出核酸扩增技术(NAT)可作为支原体检测方法的替代方法,但也提到“可采用经国家药品鉴定机构认可的其他方法”。2022年5月,国家药监局药审中心发布了《免疫细胞治疗产品药学研究与评价技术指导原则(试行)》,其中提到“当检验样品量有限,或需要快速放行等特殊情况下,如药典方法无法满足,可考虑开发新型的无菌和支原体的检测方法进行放行检测,但是新型检测方法应经过充分验证” 在日本、欧洲和美国药典中均已收录核酸扩增技术(NAT)作为支原体检测的替代方法,但需要对其进行验证,包括检测限、特异性和稳定性等方面。 |
| Takara基于核酸扩增技术(NAT)推出的支原体检测试剂盒 |
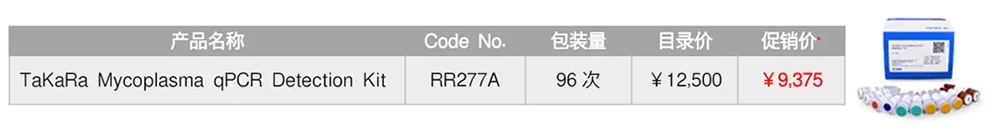 |
| *促销时间:即日起至2025年5月31日 注:本产品仅供科学研究使用,不能用于人、动物的医疗或诊断程序。 根据第18版日本药典修订的支原体检测法,对试剂盒检测限、覆盖度、特异性和稳定性进行了详细验证,证实本试剂盒可以用作核酸扩增技术(NAT)。 |
使用来自ATCC的支原体标准品,对本制品的95%阳性检出界限进行了确认。结果显示,所有被测支原体的95%阳性检出界限为10 cfu/ml或更低。 使用额外的市售支原体基因组DNA,以约10 pg的DNA作为模板,对每个样品进行qPCR检测。结果显示,无论哪个种类,都能良好检出,表明其覆盖度很高。 使用市售细菌基因组DNA,以约100 pg的DNA作为模板,对每个样品进行qPCR检测。结果显示,未检测到与任何被测细菌基因组DNA存在交叉反应,确认其特异性很高。 改变酶组分添加比例及更换检测仪器,均不会影响支原体的正常检出,证明其具有良好的稳定性。 |
| 基于qPCR的支原体检测具有更高的检测灵敏度、特异性和准确性,此外qPCR的工作流程更简化、更经济,使其成为重复常规筛查的理想选择。对于寻求简单而严格的预防性支原体筛查的机构,请考虑选择Takara支原体qPCR检测试剂盒。 |
页面更新:2025-05-14 09:19:47