| 新品┃高安全性、高效价的慢病毒包装方案新选择 | |||||||||||||||||||||||||
| 慢病毒是一种可用于在包含原代细胞、干细胞、神经细胞等非分裂细胞在内的哺乳动物细胞中进行基因导入的多用途工具。Takara推出的新品LVpro™ Packaging Mix with pLVpro系列载体可以帮助你获得高安全性、高效价的慢病毒。 | |||||||||||||||||||||||||
| ■产品介绍 | |||||||||||||||||||||||||
| LVpro Packaging Mix是经过优化的质粒混合物,高效表达慢病毒制备所需要的成分,可包装生产高滴度重组慢病毒。 | |||||||||||||||||||||||||
| pLVpro vector是tat非依赖性第三代慢病毒载体,其中5’LTR的U3区域被CMV启动子取代,并且在不影响感染滴度的情况下删除了包装信号附近的HIV来源序列。 | |||||||||||||||||||||||||
| 将pLVpro vector和LVpro Packaging Mix共转染Lenti-X 293T细胞,包装质粒瞬时表达Gag、Pol、Rev和VSV-G包膜蛋白,这有助于将重组病毒RNA(从pLVpro慢病毒载体转录而来)包入完整的病毒粒子中。使用这种经过优化的包装质粒混合物和高效转染Lenti-X 293T细胞的转染试剂Trans IT-Virus-GEN(Mirus Bio, Code No. MIR 6700)或Trans IT-293(Mirus Bio, Code No. MIR 2700),可以获得高滴度的重组慢病毒,而且在多数情况下,该病毒可用于直接感染靶细胞,而不需要事先进行浓缩处理。 | |||||||||||||||||||||||||
| ■产品特点 | |||||||||||||||||||||||||
| ·HIV-1 tat非依赖性第三代慢病毒载体 ·临床使用可能,将HIV-1来源序列排除到极限,提高安全性 ·优化了包装系统,制备高滴度慢病毒粒子 ·和3’LTR/ΔU3 pLVpro vector组合使用可进行P2实验(注:取决于插入基因) |
|||||||||||||||||||||||||
| ■实验例1 | |||||||||||||||||||||||||
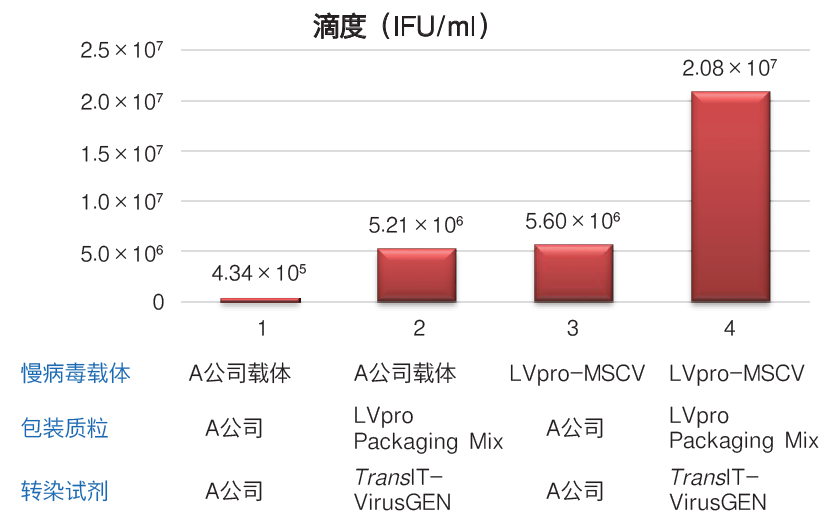
| LVpro Packaging Mix和其他品牌同类试剂盒制备的慢病毒滴度比较 | |||||||||||||||||||||||||
| 将表达ZsGreen1的慢病毒载体和包装质粒共转染Lenti-X 293T细胞制备重组慢病毒,使用HT-1080细胞评估其生物学效价。与全部使用A公司产品的场合【1】相比,部分使用Takara产品的场合【2、3】得到的慢病毒滴度要高出10倍。另外,在全部使用Takara产品的场合【4】得到慢病毒滴度是最高的。 | |||||||||||||||||||||||||
 |
|||||||||||||||||||||||||
| ■实验例2 | |||||||||||||||||||||||||
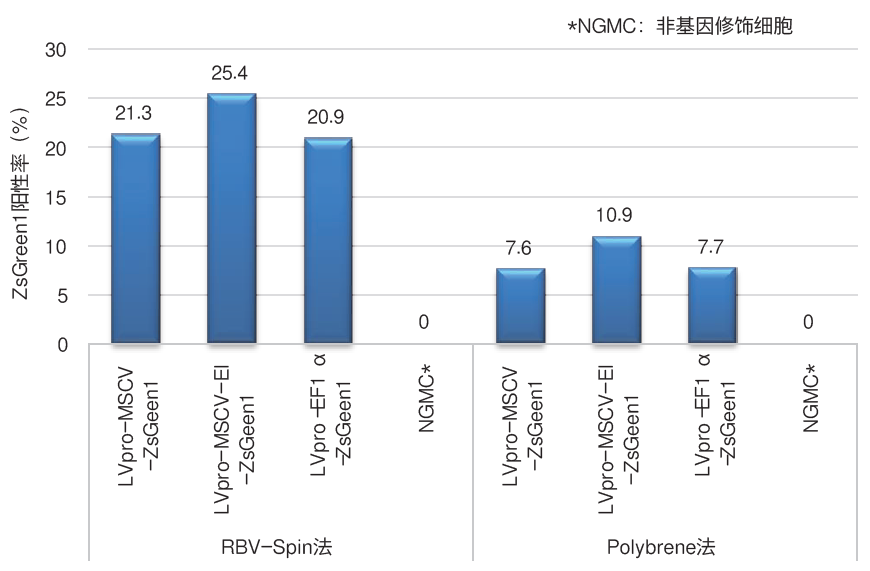
| 两种慢病毒基因导入方法比较:RBV-Spin法 vs Polybrene法 | |||||||||||||||||||||||||
| 使用LVpro Packaging Mix制备表达ZsGreen1的慢病毒并进行30倍稀释,然后分别通过RetroNectin(Code No. T100A)的RBV(RetroNectin Bound Virus)-Spin法或Polybrene法对人外周血单核细胞(PBMC)进行基因导入,比较这两种方法的转导效率。 感染3天后回收细胞,测定ZsGreen1阳性细胞率。结果显示,Polybrene法的阳性率为10%左右,而RBV-Spin法的阳性率在20%以上,与Polybrene法相比显示出较高的阳性率。 |
|||||||||||||||||||||||||
 |
|||||||||||||||||||||||||
| ■产品列表 | |||||||||||||||||||||||||
|
|||||||||||||||||||||||||
页面更新:2022-08-30 15:51:46